Effizientere Forschung in der Pathologie
Die neue, schnellere Strategie nutzt elektronenmikroskopisches SEM-Imaging für die ultrastrukturelle Analyse großer Gewebeschnitte
Die Elektronenmikroskopie ist ein unverzichtbares Werkzeug für Pathologen, da sie hochauflösende Bilder von Gewebestrukturen, Zellen, Organellen und Mikroben bereitstellt. Ultrastrukturelle Analysen großer Gewebebereiche können jedoch eine Herausforderung darstellen und zeitaufwändig sein.

Wir haben mit Dr. Mike Reichelt, einem leitenden Forscher bei Genentech, Inc. (USA) gesprochen, der im Fachbereich der Pathologie das elektronenmikroskopische Labor leitet. Dr. Reichelt entwickelt und implementiert innovative Strategien, um den Anforderungen an Forschung und Entwicklung bei Genentech gerecht zu werden.
Dr. Reichelt und seine Kollegen haben jüngst einen Artikel veröffentlicht, in dem sie für Anwendungen in der ultrastrukturellen Pathologie einen effizienten Imaging-Workflow großer Gewebeschnitte mittels Rückstreuelektronen-SEM (BSE-SEM) beschreiben.
Was war Ihr Beweggrund dafür, diesen neuen Workflow für das elektronenmikroskopische Imaging großer Gewebeschnitte zu entwickeln?
In unserem Fachbereich der Pathologie sahen wir uns mit der Notwendigkeit konfrontiert, die Analyse von gesundem oder krankem Gewebe sowohl auf histologischer als auch auf ultrastruktureller Ebene durchführen zu können. Ich konnte eine Strategie entwickeln, die sich auf die Präparation großer Gewebeschnitte (mehrere Quadratmillimeter) konzentrierte, mit Schwerpunkt auf großflächigen Bildaufnahmen. Diese großflächigen Bildaufnahmen mit geringer Vergrößerung dienen als histologische Übersichtsbilder und sind einfach mit hochaufgelösten, ultrastrukturellen Merkmalen innerhalb desselben Gewebeschnitts korrelierbar.
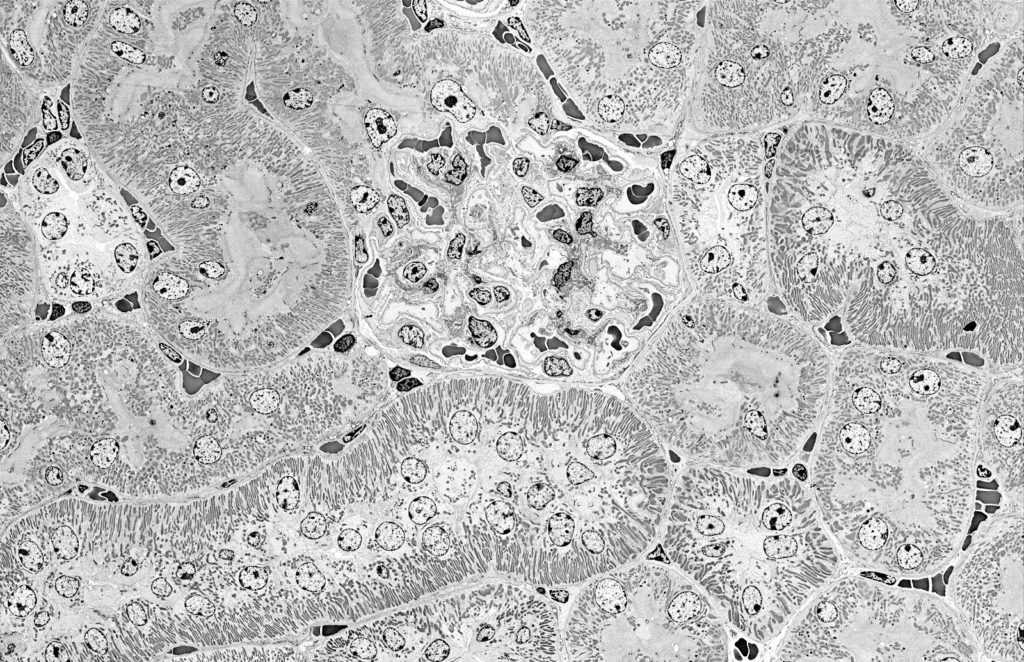
In Ihrer Strategie nutzen Sie die Rückstreuelektronen in der Rasterelektronenmikroskopie (BSE-SEM). Können Sie beschreiben, warum Sie sich für dieses Verfahren entschieden haben – gegenüber herkömmlichen Methoden?
Üblicherweise wird die ultrastrukturelle Analyse von Gewebe über Transmissionselektronenmikroskopie (TEM) durchgeführt. Obwohl dieses Verfahren seit Jahrzehnten mit großem Erfolg angewandt wird, ist es zeitaufwendig und mit vielen Hürden verbunden:
- Die geringe Größe des TEM-Trägernetzes begrenzt die Größe des Gewebeschnitts.
- Das Stützgitter im Trägernetz schränkt das Sichtfeld weiter ein und verdeckt es.
- Die Präparation ultradünner Proben erfordert eine spezielle Ausbildung und Fachpersonal.
- Es kann äußerst schwierig und zeitaufwändig sein, die hochvergrößerten TEM-Bilder mit den lichtmikroskopisch definierten Untersuchungsbereichen zu korrelieren.
Im Gegensatz dazu entfallen diese Hürden beim Imaging von Gewebe mit modernen Feldemissions-Rasterelektronenmikroskopen (FE-SEMs) in Kombination mit Probenverarbeitungsstrategien, die die Präparation großer intakter Gewebeschnitte (mehrere Quadratmillimeter) ermöglichen. Unser neuer Arbeitsablauf nutzt die sehr großen Scanfelder, die mit modernen FE-SEMs möglich sind, voll aus. Diese ermöglichen die Aufnahme großer Übersichtsbilder, die durch digitales Zoomen auch auf ultrastruktureller Ebene untersucht werden können.
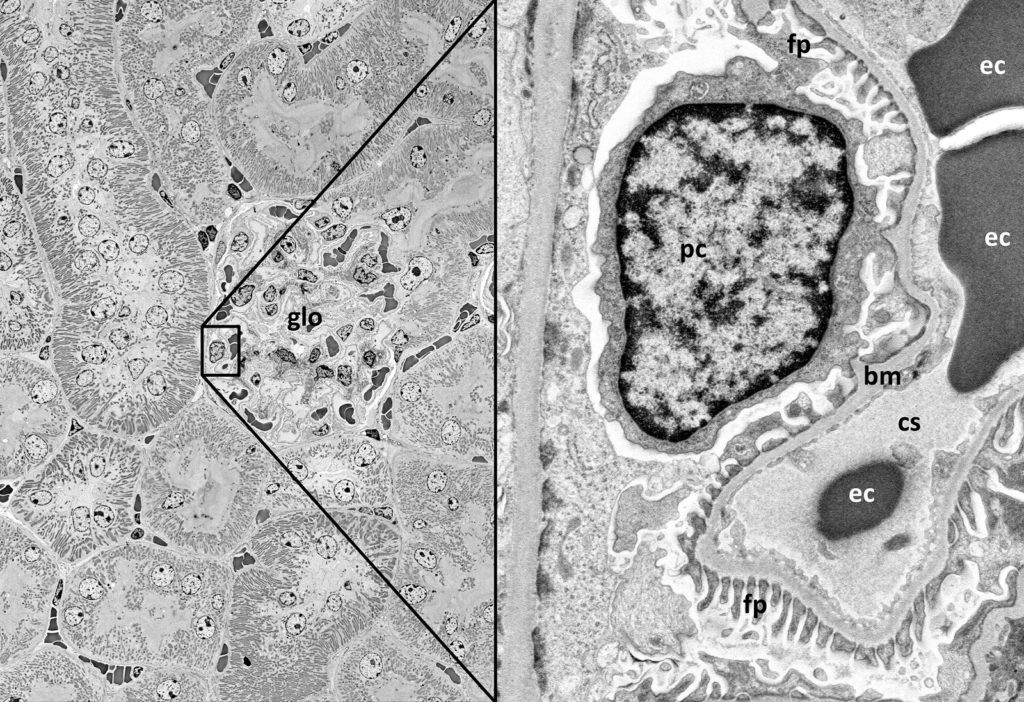
Seit seiner Einführung in unserem Labor hat dieses skalierbare Imaging mit BSE-SEM unsere ultrastrukturelle Gewebeanalyse erheblich vereinfacht und beschleunigt.
Das Imaging für die ultrastrukturelle Analyse von Gewebe (mindestens 20 Fälle pro Jahr) wird inzwischen fast ausschließlich mit ZEISS GeminiSEM 300 durchgeführt. Seit der Einführung des Verfahrens im Jahr 2018 haben wir mit diesem Verfahren bereits zu vier veröffentlichten Peer-Review-Fachartikeln beitragen können. Zahlreiche weitere Manuskripte unserer wissenschaftlichen Mitarbeiter sind gerade in Arbeit.
Wo sehen Sie im Hinblick auf neue Verfahren und Technologien die Entwicklung in Ihrem Bereich in den nächsten fünf Jahren?
Aus der Perspektive der forschenden Pathologie in der Biotech-Branche sind die drei wichtigsten Entwicklungen im Imaging für ultrastrukturelle Analysen in den nächsten fünf Jahren:
Nummer 1:
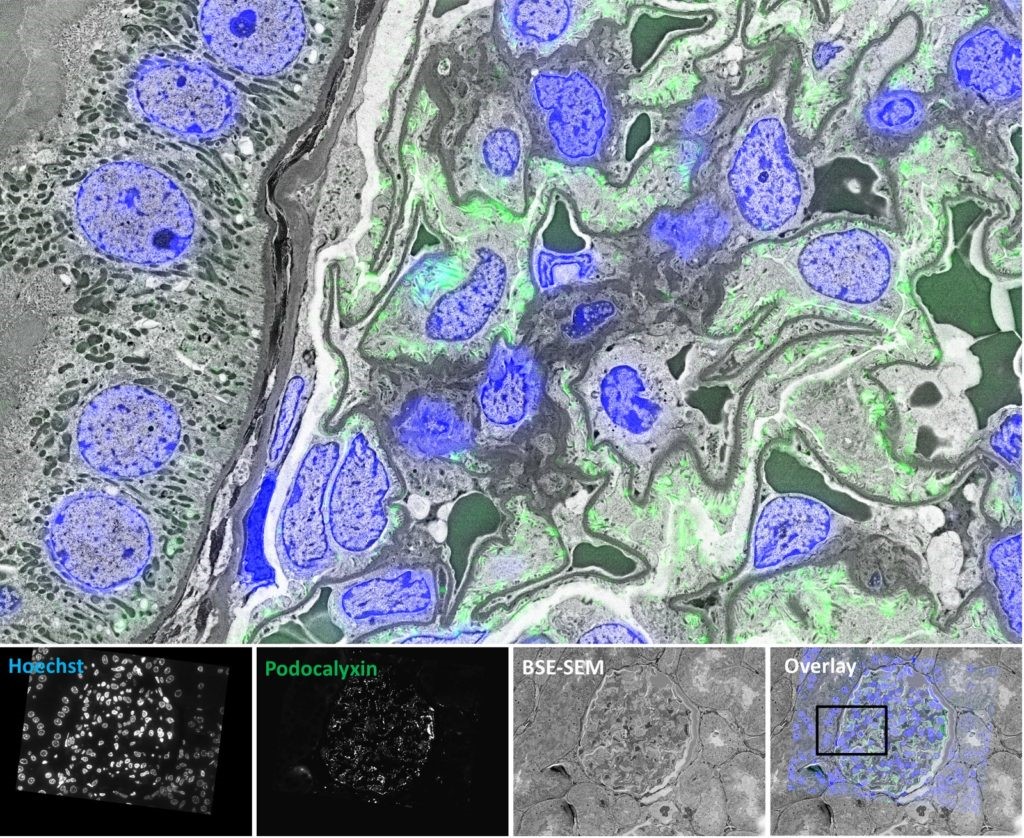
Die Einführung effizienter, korrelierter Workflows zur Kombination des elektronenmikroskopischen Imagings mit immunfluoreszenzmikroskopischen Verfahren, mit denen Zelltypen, Organellen und Arzneimitteltargets molekular charakterisiert bzw. therapeutische Moleküle lokalisiert werden. Diese Kombination ermöglicht eine ultrastrukturelle Auflösung im Kontext.
Obwohl in der Literatur bereits mehrere Strategien zum korrelierten Imaging beschrieben wurden, bestehen weiterhin Hürden, wie z. B. die Entwicklung optimierter Gewebebearbeitungsmethoden, mit denen sowohl die Antigene und die GFP-Fluoreszenz aufrechterhalten werden, ohne den Kontrast der Ultrastruktur und der Membran zu beinträchtigen. Des Weiteren fehlen weiterhin einfache Workflows für die Aufnahme und Korrelation von licht- und elektronenmikroskopischen Bildern.
ZEISS ZEN Connect, ZEISS Shuttle & Find und ZEISS Atlas sind gute Schritte, mit denen wir diesem Ziel näher kommen.
Nummer 2:
Die Interpretation, Quantifizierung und Analyse von ultrastrukturellen Bildinformationen wird erheblich beschleunigt durch neuartige Tools des “maschinellen Lernens” und der “künstlichen Intelligenz”, da diese bei der automatischen Segmentierung von ultrastrukturellen Merkmalen (z. B. Organellen) unterstützen.
Nummer 3:
Forscher werden zunehmend 3D-Datensätze für umfassendere Auswertungen und Analysen benötigen. Ich glaube, dass die Array-Tomographie von Serienschnitten, die kompatibel ist mit korrelativer Mikroskopie für Immunfluoreszenz und Ultrastruktur, sowie auch das serielle Block-Face-Imaging von großen Gewebevolumen (3View) für unser elektronenmikroskopisches Labor von größter Bedeutung sein werden.
Die elektronenmikroskopische Volumen-Methode ist üblicherweise in ihren Einsatzmöglichkeiten begrenzt, weil die Segmentierung großer Bilddatensätze extrem zeitaufwändig ist. Deshalb hat diese Technologie in der Biotech-Branche, wo Innovation mit Effizienz und hohem Durchsatz gepaart werden muss, an Bedeutung verloren. Angesichts der Fortschritte der letzten Jahre bei der Entwicklung automatisierter Segmentierungsverfahren scheint diese Einschränkung jedoch rasch zu verschwinden, sodass auch die Volumenelektronenmikroskopie wiederum zunehmend an Bedeutung gewinnen wird.
Erfahren Sie mehr zu ZEISS GeminiSEM Rasterelektronenmikroskopen.
Erfahren Sie mehr
Lesen Sie hier den vollständigen Artikel, in dem das Verfahren von Dr. Reichelt beschrieben wird.
Lesen Sie Artikel, in denen Dr. Reichelt dieses Verfahren implementiert hat:
- IRE1α disruption in triple-negative breast cancer cooperates with anti-angiogenic therapy by reversing ER stress adaptation and remodeling the tumor microenvironment. Link
- Disruption of IRE1α through its kinase domain attenuates multiple myeloma. Link
- Autophagy of Sensory Neurons in the Trigeminal and Dorsal Root Ganglia of Cynomolgus Monkeys (Macaca fascicularis). Link


